mRNA脂質(zhì)遞送載體LNP的研發(fā)處方分析 (輔助磷脂——植物膽固醇)
納米醫(yī)學(xué)網(wǎng)學(xué)術(shù)分享
近年來,脂質(zhì)納米粒(LNP)已成功作為RNA疫苗和療法的遞送平臺(tái)。裸露的RNA是一種帶負(fù)電荷的親水性大分子,由于細(xì)胞膜的靜電排斥,難以進(jìn)入細(xì)胞,且易被體內(nèi)RNA酶迅速降解。因此,需要保護(hù)性外殼才能進(jìn)入細(xì)胞。因?yàn)榧?xì)胞膜主要由脂質(zhì)組成,利用脂質(zhì)囊泡包封RNA可通過細(xì)胞膜并將RNA釋放到細(xì)胞質(zhì)中。因此,囊泡首先應(yīng)該是一種帶正電的脂質(zhì),能夠結(jié)合帶負(fù)電的RNA。然而,由陽離子脂質(zhì)組成的囊泡由于能與帶負(fù)電的細(xì)胞膜發(fā)生靜電作用而引起細(xì)胞毒性,脂質(zhì)結(jié)構(gòu)已經(jīng)發(fā)展成為能夠?qū)?nèi)體酸性環(huán)境響應(yīng)而帶正電荷的分子。
LNP的制備取決于自組裝能力,即脂質(zhì)成分發(fā)生分子間相互作用而自發(fā)組織成納米結(jié)構(gòu)實(shí)體。首先,帶負(fù)電荷的核酸和帶正電荷的脂質(zhì)之間通過靜電結(jié)合,然后,通過脂質(zhì)組分之間的疏水作用和范德華作用進(jìn)行組裝,進(jìn)而形成LNP。由于脂質(zhì)化學(xué)的多樣性、核酸的獨(dú)特性以及兩者混合的時(shí)間特性,自組裝早期階段的表征和對(duì)LNP最終性質(zhì)相關(guān)影響的研究依然具有挑戰(zhàn)性。LNP制備方案至少會(huì)在兩方面影響自組裝產(chǎn)物:LNP的均勻性和核酸負(fù)載效率。
植物性膽固醇
膽固醇是一種天然豐富的細(xì)胞膜成分,常作為LNP配方的結(jié)構(gòu)脂質(zhì)。LNP配方中膽固醇占比約20?50%。膽固醇是動(dòng)物細(xì)胞膜的豐富成分,通常從羊毛等天然原料中大量提取。膽固醇在細(xì)胞攝取中的作用很長(zhǎng)一段時(shí)間一直被忽視。研究發(fā)現(xiàn),用天然植物甾醇(如β-谷甾醇和氧化膽固醇衍生物)取代LNP配方中的膽固醇,可以顯著改善mRNA的遞送,可能由于內(nèi)吞途徑中不同的脂質(zhì)運(yùn)輸和LNP內(nèi)體逃逸的增強(qiáng)的結(jié)果。雖然目前還不完全清楚為什么含有β-谷甾醇的LNP更有可能逃脫溶酶體途徑,但它們的形狀多態(tài)性和多層結(jié)構(gòu)組織可能會(huì)使內(nèi)體膜變形或延長(zhǎng)核酸釋放的時(shí)間框架。膽固醇主要存在于LNP的外殼,這解釋了為什么對(duì)固醇結(jié)構(gòu)進(jìn)行修飾可能會(huì)引起LNP表面的組織變化。
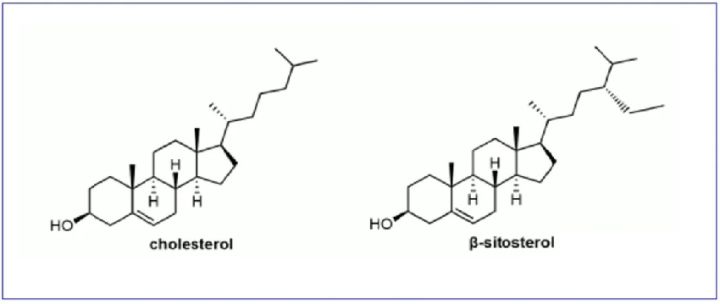
圖:膽固醇和植物性β-谷甾醇
此外,最近的研究表明,當(dāng)接觸載脂蛋白E(ApoE)時(shí),膽固醇會(huì)從LNP核心轉(zhuǎn)移到脂質(zhì)外殼上。這些結(jié)果表明,與可電離脂質(zhì)相比,雖然膽固醇相對(duì)惰性,但膽固醇及其衍生物可能影響細(xì)胞識(shí)別途徑。然而,關(guān)于LNP配方中膽固醇的修飾,仍然存在許多未知和挑戰(zhàn)。例如,植物甾醇沒有膽固醇那么豐富,供應(yīng)稀少,生產(chǎn)成本高,可能會(huì)阻礙它們?cè)?span style="font-size: 20px; line-height: 2; font-family: arial, helvetica, sans-serif;">LNP配方中的應(yīng)用;原料的性質(zhì)和相應(yīng)的痕量雜質(zhì)可能會(huì)導(dǎo)致LNP的批次差異性。固醇和脂質(zhì)的立體化學(xué)也可能對(duì)LNP配方產(chǎn)生潛在影響,如立體化學(xué)是否會(huì)影響脂質(zhì)的識(shí)別、運(yùn)輸和循環(huán)利用? 不同對(duì)映體在LNP表面的脂質(zhì)堆積是否有顯著差異? 這些問題的答案需要進(jìn)一步的研究探索。
LNPs組成成分
LNP四大組成成分相對(duì)固定:膽固醇、磷脂、PEG衍生物、陽離子脂質(zhì)。其中陽離子脂質(zhì)是靈魂,兼具充分包裹mRNA分子和促進(jìn)細(xì)胞吸收兩重作用,是LNP逃離內(nèi)體的關(guān)鍵成分。陽離子脂質(zhì)與帶負(fù)電的 mRNA 結(jié)合,可高效包載核酸藥物,同時(shí)提供正電荷,與帶負(fù)電荷的mRNA復(fù)合,有助于內(nèi)涵體逃逸。常用的產(chǎn)品有DLin-MC3-DMA,DOTAP.Cl,DC-CHOL等。而聚乙二醇化磷脂可提高粒子穩(wěn)定性,減少粒子在體內(nèi)與血漿蛋白的結(jié)合,延長(zhǎng)體循環(huán)時(shí)間。例如DMG-PEG2000,DSPE-MPEG2000。新冠疫苗中, Moderna和 BioNTech基本成分一樣,陽離子脂質(zhì)(Moderna)與聚乙二醇脂質(zhì)(BioNTech)結(jié)構(gòu)極其相似,各組分比例近似,它們用到的脂質(zhì)體還包括ALC-0159,cholesterol,ALC-0315,DSPS,SM-102等
北京天優(yōu)福康生物科技有限公司
官網(wǎng):http://www.jyzjsd.com/
服務(wù)熱線:400-860-6160
聯(lián)系電話/微信:13718308763
QQ:2136615612 3317607072
E-mail:Tianyoubzwz@163.com


